Desvendados estágios iniciais da doença de Parkinson
Redação do Diário da Saúde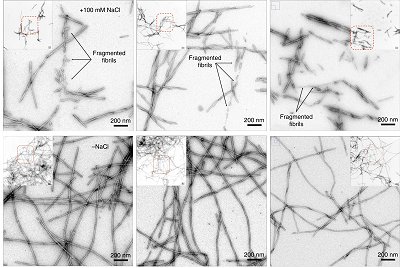
[Imagem: Guilherme Oliveira/Jerson Silva]
Como começa o Parkinson
Usando técnicas de ponta em microscopia eletrônica, cientistas do Brasil e dos EUA identificaram estruturas proteicas que podem explicar o início precoce da doença de Parkinson.
Uma das maiores dificuldades no tratamento contra a doença neurodegenerativa progressiva é a falta de entendimento sobre o momento exato em que a enfermidade começa a se desenvolver.
Agora, pesquisadores da UFRJ (Universidade Federal do Rio de Janeiro) e da Universidade da Virgínia (EUA) observaram, pela primeira vez, como diferentes variantes da alfa-sinucleína, proteína associada à enfermidade, interagem ao longo do tempo.
A partir disso, eles conseguiram identificar a formação inicial de agregados da proteína ligados aos casos precoces do Parkinson.
Compreender como essas estruturas se organizam é fundamental para identificar os estágios iniciais da doença. Já se sabe que a degeneração dos neurônios que leva ao aparecimento dos sintomas, como tremores e lentidão dos movimentos, está ligada ao acúmulo de agregados da alfa-sinucleína no cérebro, os chamados filamentos amiloides.
Antes de formarem tais filamentos, as proteínas passam por um estágio intermediário, os oligômeros, que também estão presentes nos cérebros dos pacientes com Parkinson. Apesar de conhecerem essas estruturas, os cientistas ainda não compreendem como seu surgimento se dá, nem seus graus de toxicidade para os neurônios.
"Uma pessoa desenvolve Parkinson ao longo de toda a vida. A conversão entre os estágios da proteína acontece lentamente e as estruturas intermediárias e os filamentos se acumulam por muito tempo. E não sabemos qual dos dois desencadeia o surgimento dos sintomas e é mais tóxico para as células," explicou o pesquisador Guilherme de Oliveira. "Se conseguirmos entender o início da conversão, poderemos desenvolver uma terapia para o tratamento precoce da doença."
Alfa-sinucleína
Os cientistas compararam a dinâmica de formação dessas neuroestruturas em quatro variantes da alfa-sinucleína, sendo três delas ligadas a casos hereditários precoces da doença de Parkinson e uma presente nos casos de envelhecimento. A partir daí, eles observaram diferenças significativas nos processos de agregação de cada variante da proteína e descobriram que, nos casos de Parkinson precoce, os estágios intermediários se formam em uma velocidade muito maior do que nos casos de envelhecimento. Isso pode explicar o surgimento dos sintomas em pessoas mais jovens.
Os pesquisadores também encontraram evidências de quais tipos de proteína são importantes para o surgimento dos filamentos amiloides e, mais do que isso, que os filamentos apresentam estruturas distintas, dependendo da variante da proteína da qual se originam.
"O interessante é que não só os estágios iniciais da conversão são diferentes, mas que alguns filamentos que se formam em casos de Parkinson precoce também são. Dependendo da mutação presente, esses filamentos se torcem de formas diferentes," explicou Jerson Lima Silva, membro da equipe.
Artigo: Alpha-synuclein stepwise aggregation reveals features of an early onset mutation in Parkinsons disease
Autores: Guilherme A. P. de Oliveira, Jerson L. Silva
Publicação: Communications Biology
Vol.: 2, Article number: 374
DOI: 10.1038/s42003-019-0598-9
| Ver mais notícias sobre os temas: | |||
Neurociências | Cérebro | Memória | |
| Ver todos os temas >> | |||
Descoberta uma forma inteiramente nova de vida dentro dos seres humanos
Mangas melhoram a sensibilidade à insulina e o controle da glicose no sangue
Emoções positivas e sono profundo melhoram a retenção da memória
Ciência desbanca conceito de meritocracia
Revolução na dermatologia e cosmética: Ciência estava errada sobre colágeno da nossa pele
Bactérias invadem cérebro após implante de chips neurais
IA descobre conexões ocultas entre doenças
Cientistas identificam 15 motivações básicas do comportamento humano
Evolução não é cega e nem aleatória: Há uma "previsão" na evolução
Fundações da inteligência humana são observadas pela primeira vez
Menor marcapasso do mundo é ativado por luz, sem fios
Usar o celular antes de dormir piora a qualidade do sono
Esponjas de seda substituem cobaias e revolucionam diagnóstico do câncer
Estimulação nervosa é eficaz quando sincronizada com ritmos do corpo
Dançar afasta o estresse e traz vários outros benefícios
Estimulação elétrica neuromuscular aumenta massa muscular e força
Ser nostálgico faz você ter mais amigos próximos
Ficamos mais próximos do controle natural de membros robóticos
Banho de chuveiro com bolhas ultrafinas cura problemas de pele
Revolução na dermatologia e cosmética: Ciência estava errada sobre colágeno da nossa pele
Vacina do Butantan contra dengue grave tem 89% de proteção
Brasil tem primeiras mortes por febre oropouche no mundo
Censo 2022: Por que várias cidades brasileiras tiveram diminuição da população?
Brasil tem primeiro caso de gripe aviária em aves domésticas
Brasil decreta emergência zoossanitária devido à gripe aviária
Proibido o uso de animais em pesquisas de cosméticos e higiene pessoal
A informação disponível neste site é estritamente jornalística, não substituindo o parecer médico profissional. Sempre consulte o seu médico sobre qualquer assunto relativo à sua saúde e aos seus tratamentos e medicamentos.
Copyright 2006-2025 www.diariodasaude.com.br. Todos os direitos reservados para os respectivos detentores das marcas. Reprodução proibida.


